
咨询热线:
17715390137
18101240246
18914047343
邮件:mxenes@163.com
扫码关注或微信搜索公众号:
二维材料Fronrier
关注后点击右下角联系我们,
进入企业微信。
专业服务在线

椎间盘变性(IDD)是脊柱疾病的主要成因。以往研究表明,铁消亡引起的髓核(NPC)衰老在 IDD 发病机制中起着关键作用。这强调了抑制铁磷灭症和延缓 NPC 衰老的治疗策略。间充质干细胞衍生的外泌体(MSC-EVs)作为一种再生纳米疗法,继承了亲本的生物特性。本研究通过模拟衰老微环境对 MSC 进行预处理,获得具有增强靶向和抗衰老特性的“驯化囊泡”(D-EVs)。多组学分析显示,D-EV 富含 GPX4 蛋白,并通过 CXCL10-CXCR3 趋化因子轴实现对衰老 NPC 的特异性结合。功能上,D-EVs 将 GPX4 蛋白传递给受体 NPC,从而抑制铁剥坏并缓解细胞衰老。为了在退行性微环境中实现持续且按需释放,我们通过 ROS 响应肽将 D-EV 锚定在热敏感水凝胶上。这种对 ROS 反应的水凝胶进一步增强了 D-EVs 在缓解 NPC 铁剥蚀和逆转衰老相关代谢功能障碍方面的疗效。体外和体内实验均显示,该针对衰老的系统显著抑制铁剥蚀和衰老途径,并阻止 NPC 衰老表型的转变。本研究提出了一种抑制铁消亡的新方法,从而延缓 NPC 衰老并减轻 IDD 的进展。

该研究以题为“Microenvironment-educated MSC-EVs loaded injectable smart hydrogel for targeting senescent nucleus pulposus cells and inhibiting ferroptosis against intervertebral disc degeneration”发表在Bioactive Materials上。
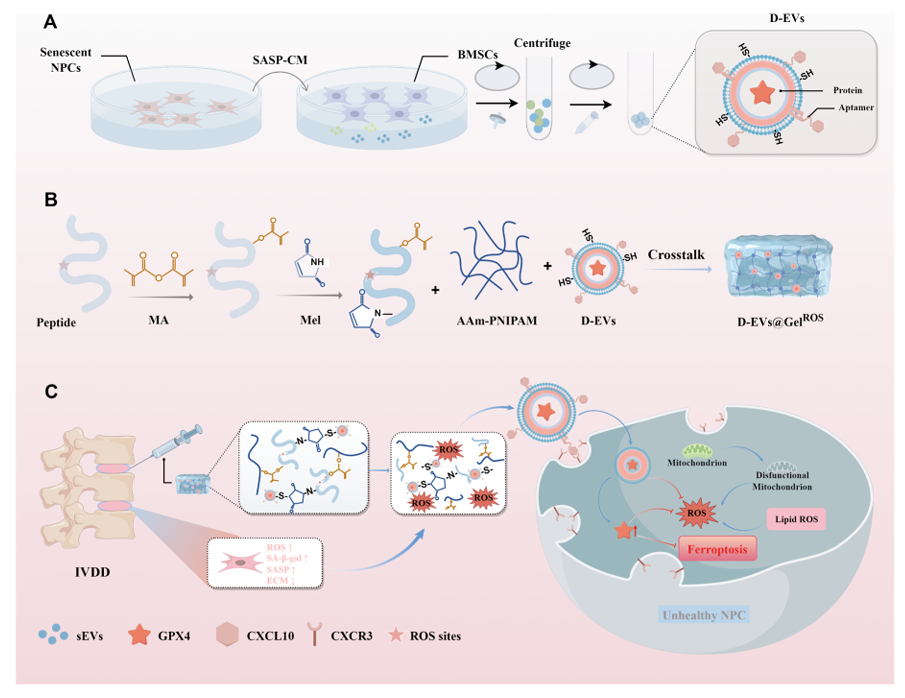
载抗衰老d - ev水凝胶的制备及调控机理示意图。A.抗衰老d - ev的驯化及提取工艺。B.合成D-EVs@GelROSwith衰老靶向能力的D-EVs@GelROSSchematic表示和ros响应官能团修饰。c .通过靶向GPX4递送改善NPC铁下垂,改善IDD
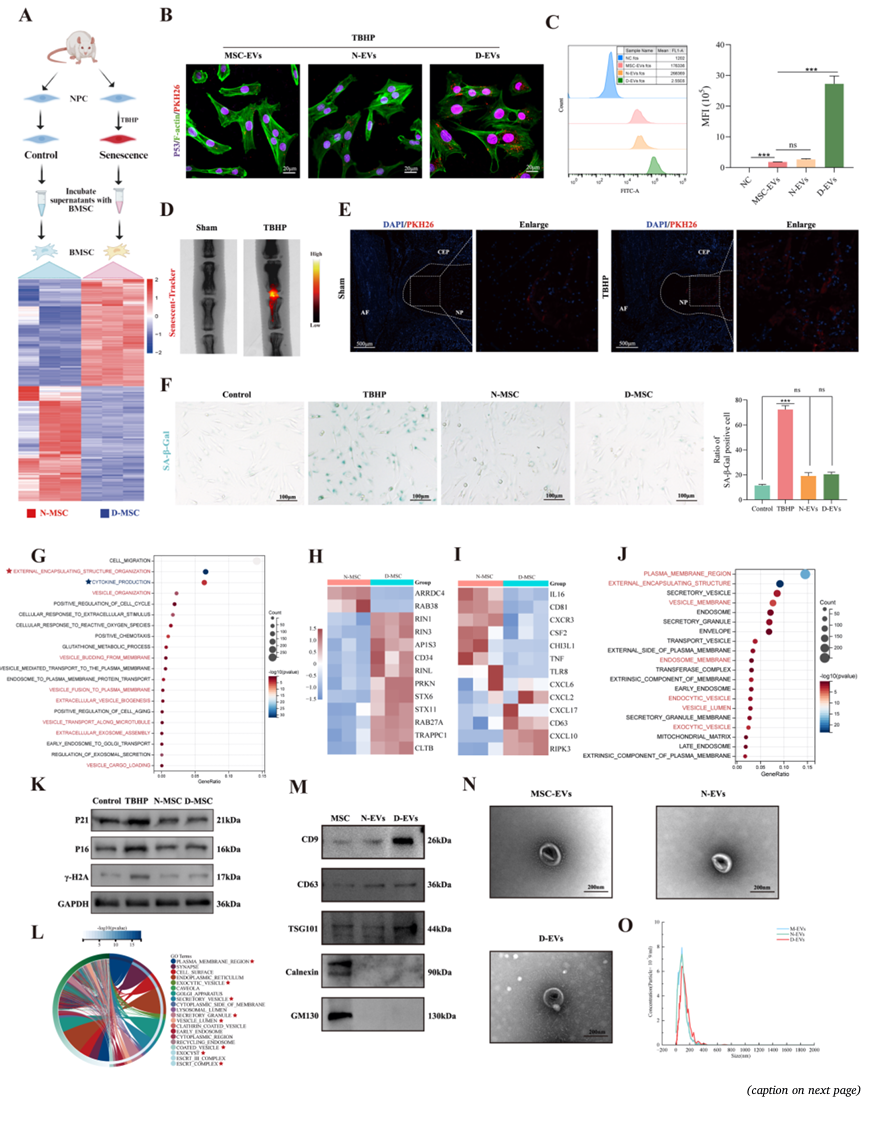
微环境诱导的衰老间充质干细胞释放高亲和力的衰老NPC驯化细胞外囊泡。(A) SASP-CM培养MSCs生成d - ev和n - ev的实验装置示意图。(B)共聚焦显微镜图像显示体外12小时后衰老NPCs的evs内化情况不同。(C)衰老npc不同ev摄取的流式细胞术和定量分析。(D)衰老生态位的体内验证。注射衰老示踪剂后的代表性荧光图像(红色)。(E)体内pkh26标记的d - ev跟踪。(F)有代表性的SA-β-Gal图像和未经过SASP-CM处理的MSCs的定量。(G)基因本体(GO)分析证实了生物过程(BP)类别中外部包封结构组织和细胞因子生产的富集。(H) D-MSCs和N-MSCs中与EVs生物发生相关的基因表达热图。(I) D-MSCs和N-MSCs中与细胞因子产生相关的基因表达的热图。(J和L)基因本体(GO)分析证实了细胞组分(CC)类别中与囊泡组织和运输相关的术语的富集。(K) Western blot分析证实了N-MSC和D-MSC中存在核心衰老标记p16和p21以及DNA损伤标记γ-H2AX。(M) Western blot分析证实CD9、CD63、TSG101、Calnexin和GM130在MSC-EVs、N-EVs和D-EVs中表达。(N) TEM图像显示msc衍生ev, N- ev和d - ev的形态和大小。(O) nta显示了msc - ev、n - ev和d - ev的尺寸分布。数据以mean±SD表示。N = 3, ns,不显著;*p < 0.05, **p < 0.01, ***p < 0.001。
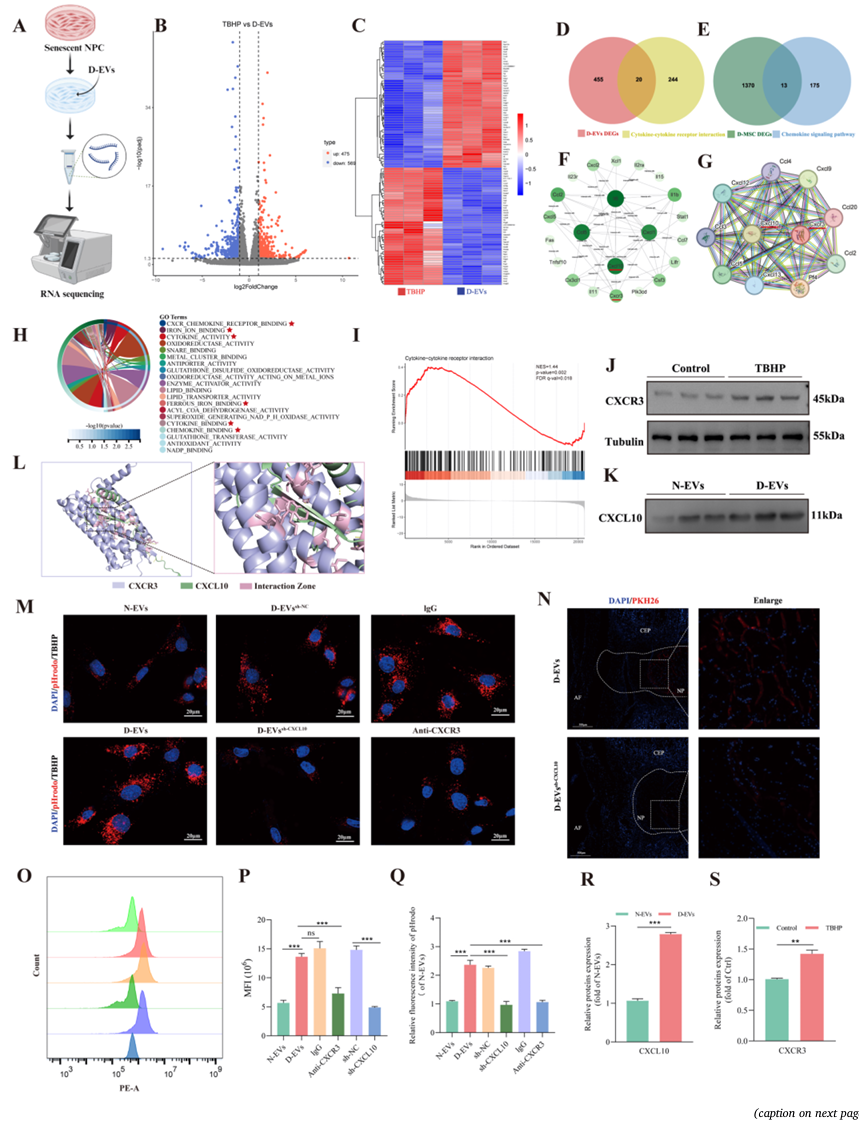
d - ev对衰老npc的靶向能力由CXCL10-CXCR3轴介导。(A)有无d - ev处理的衰老npcrna测序示意图。(B-C)火山图和热图显示了d - ev处理或未处理的衰老npc的差异基因表达。(D) Venn图显示了D- ev处理的衰老npc中鉴定的deg与细胞因子-细胞因子受体相互作用的关键基因数据库之间的重叠。(E) Venndiagram显示了在D-MSCs中鉴定的deg与趋化因子信号通路关键基因数据库之间的重叠。(F-G)以上总deg中轮毂基因的网络分析。在STRING数据库中建立蛋白-蛋白相互作用网络,利用Cytoscape软件确定网络中的hubgenes。(H)氧化石墨烯分析证实,与d - ev处理的衰老npc相关的术语在BP类别中富集。(1) GSEA分析D-EVs组与TBHP组细胞因子-细胞因子受体相互作用。(J) Western blot分析证实了CXCR3在对照和衰老npc中的表达,(S)定量分析。(K) Western blot分析证实CXCL10在N-EVs和D-EVs中表达,(R)定量分析。(L) PyMOL分析CXCR3和CXCL10的蛋白结合。(M)共聚焦分析衰老npc在n - ev、d - ev和CXCL10敲除/抗cxcr3处理后对phrodo标记ev的摄取情况,(Q)定量分析。(N) pkh26标记的CXCL10敲除d - ev的体内跟踪。(O)流式细胞术显示衰老npc对CXCL10敲除/抗cxcr3的不同ev的摄取,以及(P)定量分析。数据以mean±SD表示。N = 3, ns,不显著;*p < 0.05, **p < 0.01, ***p < 0.001。
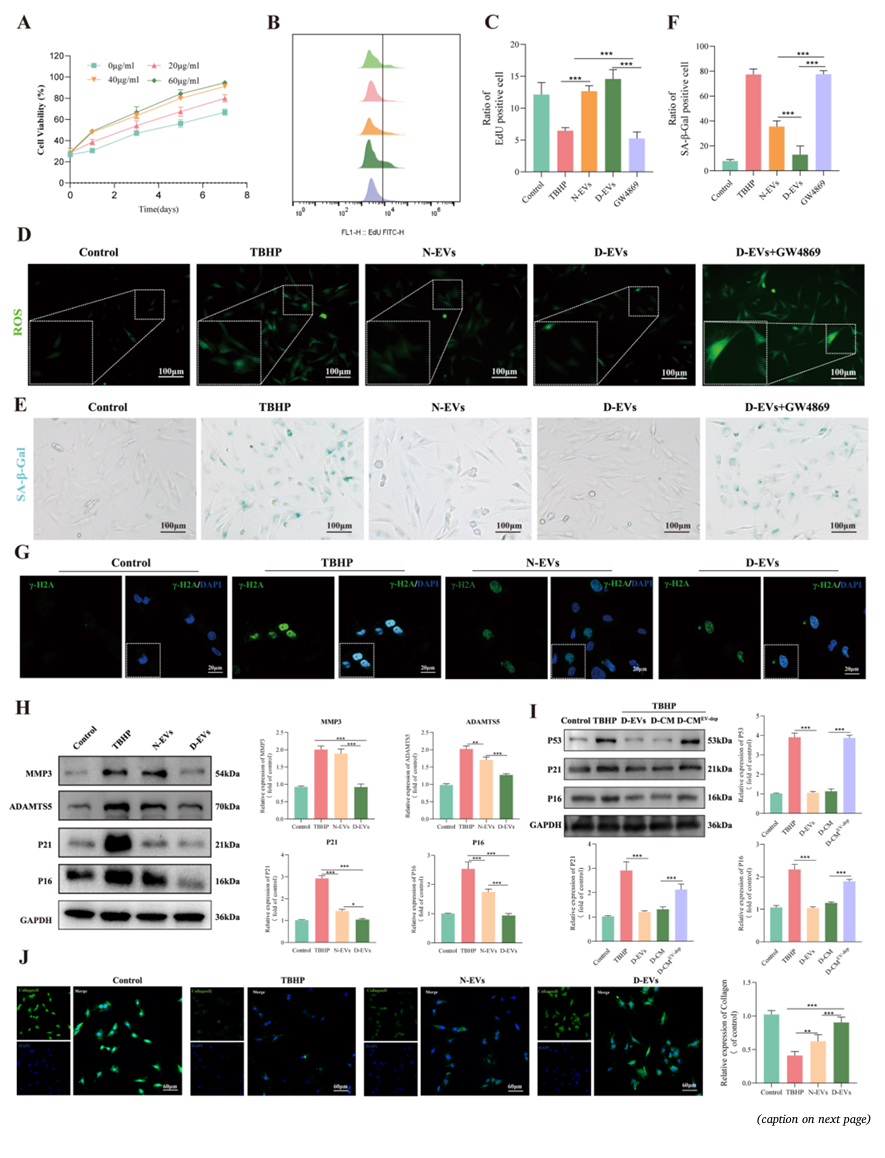
d - ev减轻细胞衰老,恢复衰老npc的ECM合成代谢/分解代谢。(A) CCK8法测定d - evs浓度对细胞活力的影响。(B)流式细胞术分析上述各组细胞增殖能力,(C)定量分析。(D) n - ev、D- ev或D- ev + GW4869处理的衰老npc的代表性ros图像。(E) n - ev、d - ev或d - ev + GW4869处理的衰老npc的代表性SA-β-Gal图像,(F)定量分析。(G) γ-H2A共聚焦分析,IF染色描绘了对照组、TBHP组、N-Evs组和D-EVs组的DNA损伤。(H)对照、TBHP、N-Evs或D-EVs治疗后npc中ECM代谢相关蛋白和衰老相关蛋白的WB分析。(I)用d - ev、D-CM或d - cmev - deep处理的衰老npc中p53、p21和p16的Western blot分析。(J)对照组、TBHP组、N-EVs组和d - evs组的COL2共聚焦分析。数据以mean±SD表示。N = 3, ns,不显著;*p < 0.05, **p < 0.01, ***p < 0.001。
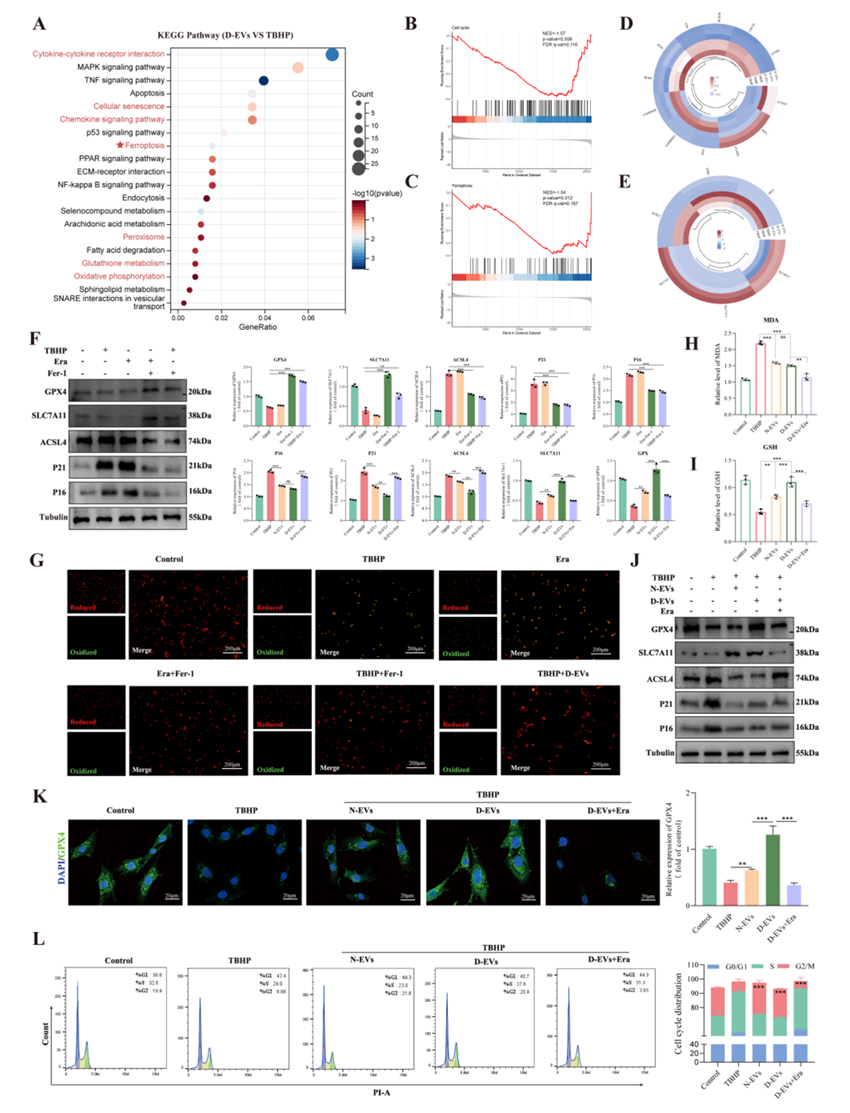
d - ev通过抑制铁下垂来对抗鼻咽癌衰老。(A)是否给予d - ev治疗后衰老npc中DEGs的KEGG通路分析。(B-C) GSEA图显示衰老npc中铁下垂和细胞周期显著富集。(D-E)参与铁氧化和细胞周期的关键基因的热图定量。(F)不同实验条件下NPCs中关键铁下垂(GPX4、SLC7A11、ACSL4)和衰老(p21、P16)标记物的Western blot分析。(G)对照、TBHP、Era、Era + Fer-1、或TBHP + Fer-1组C11-BODIPY 581/591检测脂质过氧化的代表性图像(绿色)。(H-I)对照、TBHP、n - ev、d - ev或d - ev + Era组丙二醛(MDA)水平(H)和谷胱甘肽(GSH)水平(I)的定量评估。(J) PBS、n - ev、d - ev或d - ev + Era处理后NPCs中关键铁下垂(GPX4、SLC7A11、ACSL4)和衰老(p21、P16)标志物的Western blot分析。(K)对照组、TBHP组、N-Evs组、D-EVs组和D-EVs + Era组GPX4 IF染色共聚焦分析。(L)上述实验条件下细胞周期分布的流式细胞术分析。实验组与tbhp诱导组进行统计学比较。数据以mean±SD表示。N = 3, ns,不显著;*p < 0.05, **p < 0.01, ***p < 0.001。
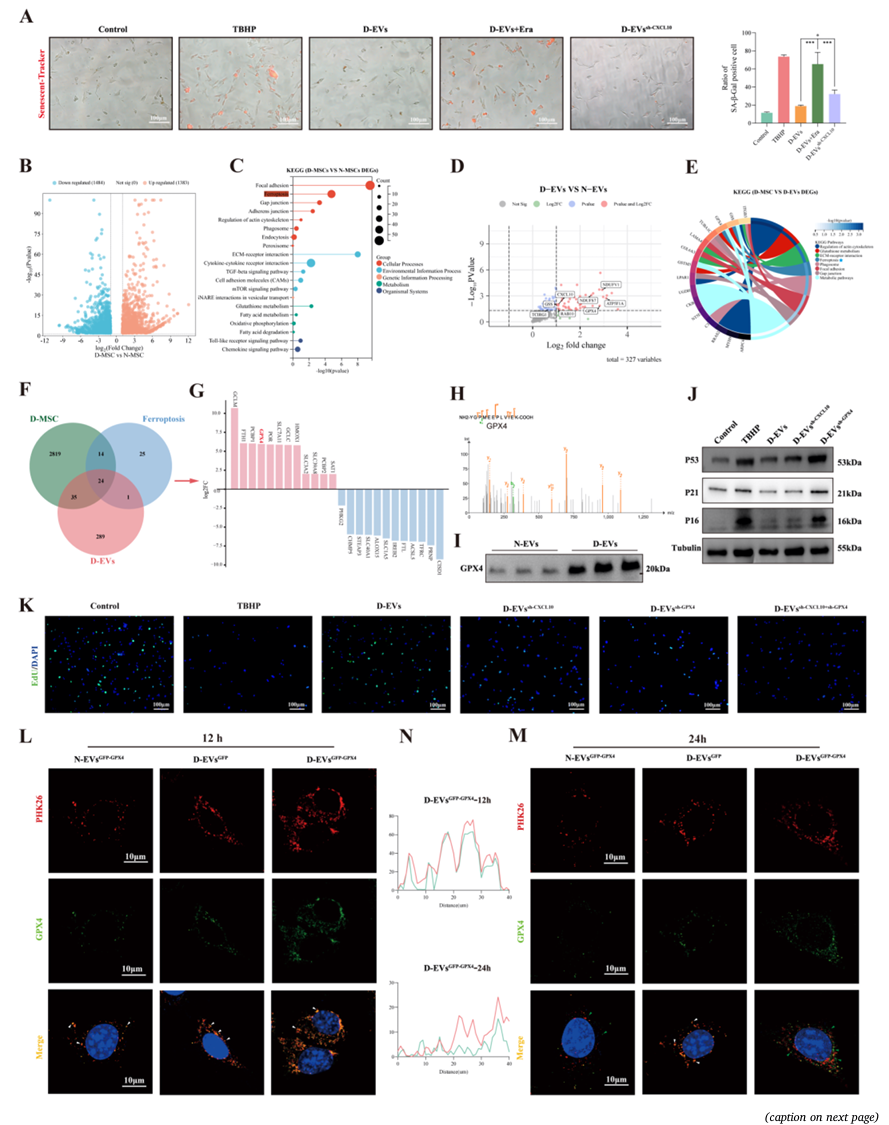
d - ev传递GPX4抑制衰老npc铁下垂(A) n - ev、d - ev、Era和d - ev处理的npc的代表性衰老跟踪器图像。(B)比较D-MSC和N-MSC转录组数据的火山图。(C) D-MSCs与N-MSCs中DEGs的KEGG通路分析。(D)比较D- ev和n - ev蛋白质组学数据的火山图。(E)转录组学和蛋白质组学数据整合的KEGG通路分析。(F)维恩图,显示了D-MSC转录组、D-EVs蛋白质组和铁凋亡相关基因集的基因交叉。(G)柱状图显示(F)中鉴定的核心重叠基因的相对表达水平。(H)质谱分析显示GPX4在D-EVs蛋白质组中富集。(1) Western blot分析证实GPX4蛋白在d - evs和N-EVs中存在。(J) Western blot分析PBS或N-EVs敲除CXCL10或GPX4后NPCs中关键衰老标志物(p21, P16)。(K)对照组、TBHP组、d - ev组、d - evsh - cxcl10组、d - evsh - gpx4组和d - evsh - cxcl10 + gpx4组细胞增殖能力的EdU代表性图像。(L-M)共聚焦图像显示不同电动汽车在共培养12小时和24小时时向衰老npc递送GPX4, (N)共定位分析。数据以mean±SD表示。N = 3, ns,不显著;*p < 0.05, **p < 0.01, ***p < 0.001。
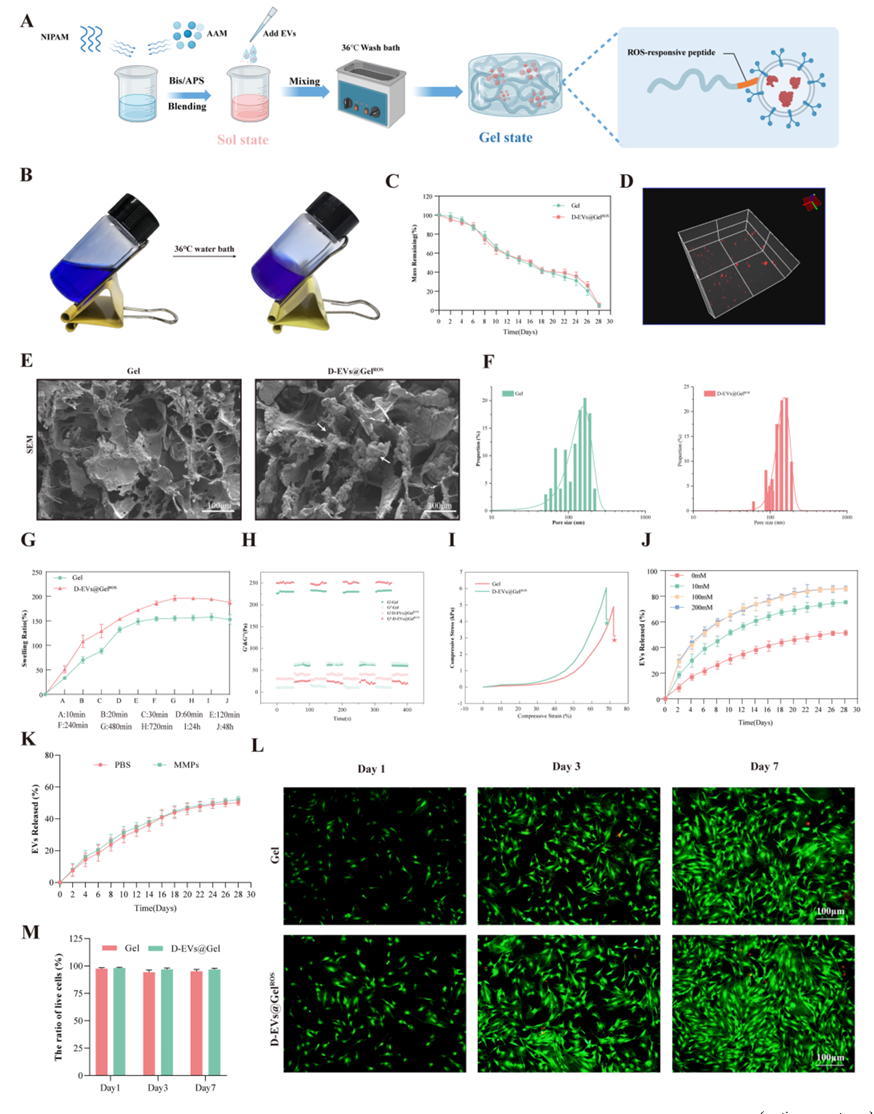
活性氧反应水凝胶的合成与表征D-EVs@Gel。(A) ros响应智能水凝胶制备工艺示意图(B) D-EVs@GelROSformulation热敏溶胶-凝胶转变的照片。(C)空白凝胶和D-EVs@Gelcollagenase的降解曲线。(D)共聚焦显微镜显示phk26标记的ev(红色)在D-EVs@GelROSROSunder内的空间分布。(E) Geland的代表性SEM图像D-EVs@GelROS。(F)凝胶粒度分布图和D-EVs@Gel48 h。(h)凝胶和D-EVs@GelROSROS的流变学测量。(G)凝胶和D-EVs@GelROSin PBS在高(20%)和低(0.1%)剪切交替作用期间的溶解度特性。(1)凝胶和D-EVs@GelROS压缩试验。(J)含有不同Hprofile的PBS与不含Hprofile的PBS孵育D-EVs@Gel中ev的累积释放曲线。(K)累积释放与含有MMP3/MMP13的PBS孵育或不含。(L)活/死细胞荧光图,(M)凝胶和D-EVs@GelROS细胞毒性的定量评估。
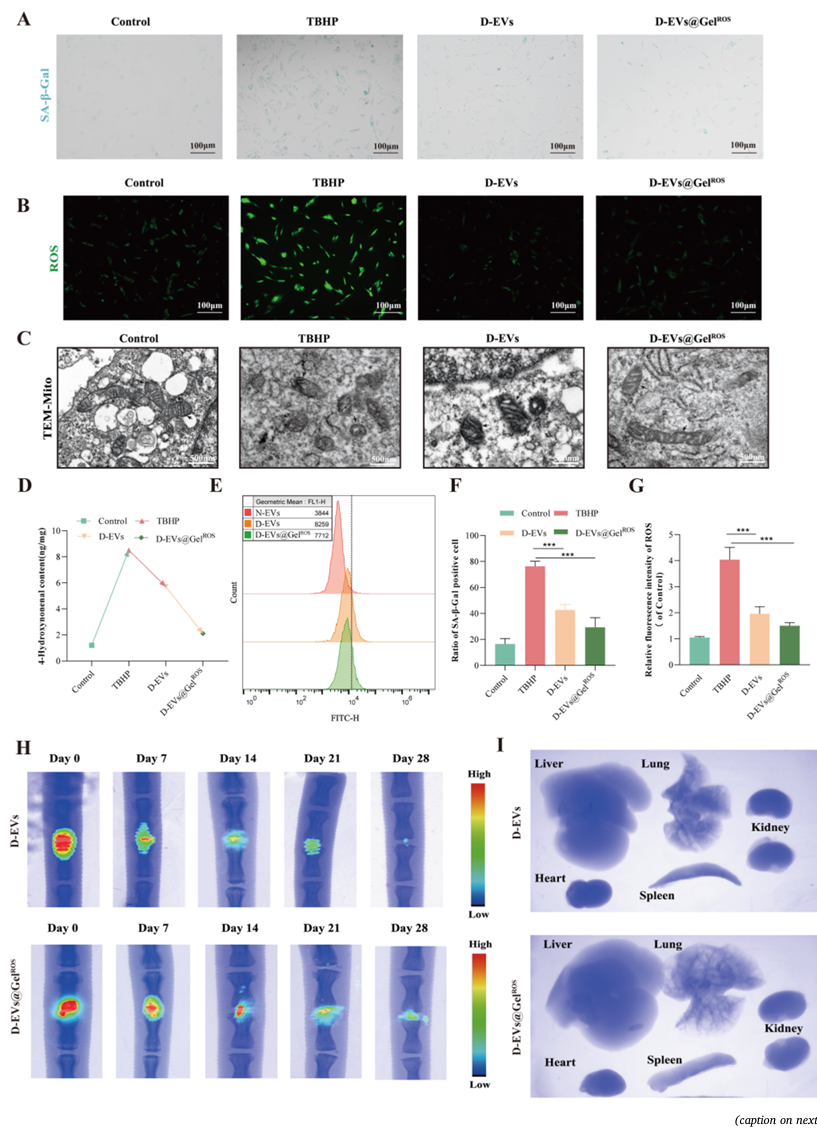
ros响应水凝胶释放d - ev的功能验证D-EVs@Geland D-EVs@GelROSROS。(A) d - ev处理的衰老npc的代表性ROS图像,(F)定量分析。(B) d - ev和D-EVs@Gelanalysis处理的衰老npc的代表性SA-β-Gal图像。(C) d - ev和D-EVs@GelROSROS处理的衰老鼻咽癌线粒体的代表性TEM图像,(G)定量。箭头表示健康的、延长的线粒体与萎缩的、浓缩的线粒体。(D)用ELISA法定量分析D- evs和D-EVs@GelROS处理的npc中4-HNE蛋白加合物的含量。(E)流式细胞术分析衰老npc对pkh26标记囊泡的摄取效率。(H)大鼠椎间盘内注射phk26标记的d - ev和D-EVs@GelROS后28天的体内荧光成像。(I) d - evs组和D-EVs@GelROS组第28天主要器官(心、肝、脾、肺、肾)的离体荧光成像。数据以mean±SD表示。N = 3, ns,不显著;*p < 0.05, **p < 0.01, ***p < 0.001。
总结
一篇发表于《Bioactive Materials》的研究开发了一种基于微环境驯化间充质干细胞外泌体(D-EVs)与活性氧响应性水凝胶(D-EVs@GelROS)的智能递送系统,用于靶向干预椎间盘退变(IDD)。研究团队首先利用衰老髓核细胞(NPCs)的条件培养基驯化间充质干细胞,获得具有增强靶向性与抗衰老功能的驯化外泌体(D-EVs)。多组学分析表明,D-EVs通过CXCL10-CXCR3趋化因子轴实现对衰老NPCs的特异性识别与内化,并富集了关键抗铁死亡蛋白GPX4。功能上,D-EVs通过直接递送GPX4蛋白抑制脂质过氧化,阻断铁死亡驱动的衰老进程,恢复NPCs的增殖能力与细胞外基质合成代谢。
为实现D-EVs在退变微环境中的长效与可控释放,研究进一步构建了基于温敏与ROS响应性肽段交联的水凝胶递送平台D-EVs@GelROS。该体系在IDD高ROS微环境中实现响应性释放,显著延长D-EVs在椎间盘局部的滞留时间,并保持其生物学活性与靶向能力。在大鼠IDD模型中,D-EVs@GelROS系统有效抑制了NPCs衰老与铁死亡标志物表达,恢复了髓核区域的结构完整性,并通过上调GPX4与COL2表达改善细胞外基质代谢,显著延缓椎间盘退变进程。该研究构建了“驯化-靶向-控释”三位一体的治疗策略,为靶向铁死亡-衰老轴治疗IDD提供了新范式。
参考消息:
DOI: 10.1016/j.bioactmat.2026.02.030
 |
 |
 |
 |
| 二维材料Frontier | 生物纳米材料前沿 | MXenes Frontier | 纳米医学Frontier |
|
版权所有 © 2019 北京北科新材科技有限公司
All rights reserved. 京ICP备16054715号-2 |
扫一扫