
咨询热线:
17715390137
18101240246
18914047343
邮件:mxenes@163.com
扫码关注或微信搜索公众号:
二维材料Fronrier
关注后点击右下角联系我们,
进入企业微信。
专业服务在线

本文精选
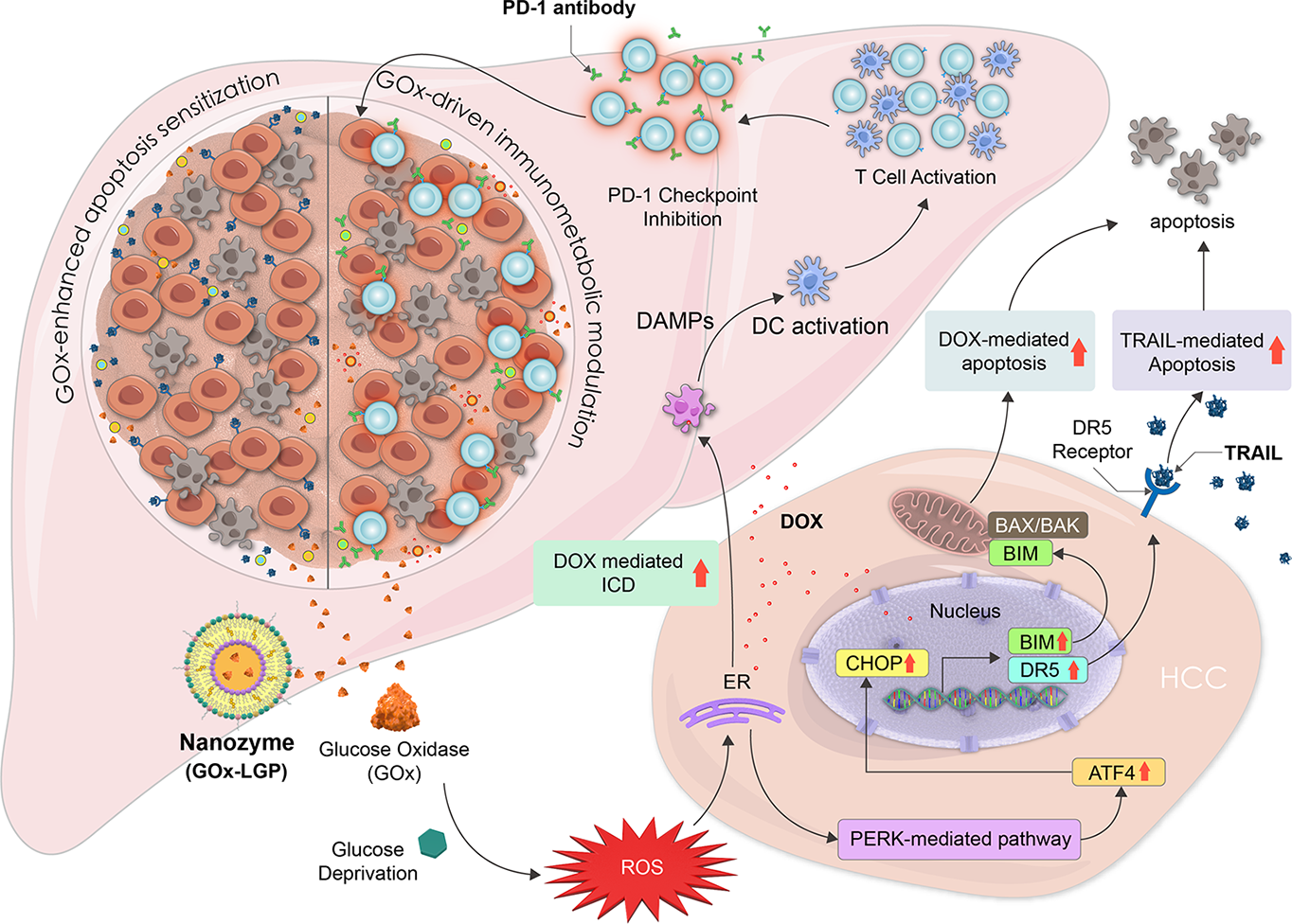
肝细胞癌(HCC)表现出深度的糖解重编程,驱动肿瘤生长、损害细胞凋亡并抑制免疫反应,导致对传统疗法产生耐药性。为克服这一挑战,我们开发了一种刺激响应纳米酶,由 pH 敏感的脂质-明胶-蛋白胨(LGP)纳米凝胶包裹葡萄糖氧化酶(GOx)组成。这种肿瘤选择性纳米酶在酸性条件下消耗肿瘤内葡萄糖,诱导氧化和内质网应激,上调死亡受体,并使肝细胞细胞对 TRAIL 和多柔比星(DOX)诱导的凋亡敏感。GOx 和 DOX 在纳米酶中的共递送重编程肿瘤免疫代谢,增强免疫原性细胞死亡并促进损伤相关分子模式(DAMPs)的释放。这些变化刺激树突状细胞成熟和细胞毒性 CD8+T 细胞激活。转录组分析证实,该纳米酶通过抑制代谢途径并激活免疫相关基因程序,重塑免疫抑制微环境。当与抗 PD-1 检查点阻断结合时,该纳米酶能在正位 HCC 模型中诱导强效肿瘤退化,并消除转移且无全身毒性。总体而言,这项工作引入了一种多功能肿瘤响应纳米酶,整合了代谢干预、凋亡启动和免疫激活,以克服 HCC 中的治疗耐药性。
思路延伸
1.平台技术的普适性探索:基于LGP纳米凝胶的刺激响应平台可被视为一个模块化系统。未来研究可探索负载其他代谢酶(如精氨酸酶、过氧化氢酶)或不同作用机制的药物(如靶向药、免疫激动剂),用于治疗其他同样依赖特定代谢途径或具有免疫抑制微环境的实体瘤,如胰腺癌、三阴性乳腺癌等。
2.联合疗法策略的进一步优化:本研究已展示了与抗PD-1联用的效果,后续思路可延伸至与其他免疫疗法(如CTLA-4抑制剂、CAR-T细胞疗法)或新兴疗法(如溶瘤病毒、肿瘤疫苗)的协同。同时,可深入研究纳米酶治疗后的肿瘤免疫景观变化,以发现新的免疫检查点或联合靶点,实现更精准的序贯或组合治疗。
3.临床转化前的重要考量:尽管动物实验效果显著,但迈向临床仍需系统评估该纳米酶的长周期生物安全性、体内代谢途径、规模化生产工艺及质量控制标准。此外,探索非侵入性影像学方法(如基于代谢变化的PET成像)来实时监测纳米酶的体内分布和治疗反应,对于未来临床精准应用具有重要价值。
原文链接
Stimuli-Responsive Nanozyme Reprograms Tumor Immunometabolism and Overcomes Therapeutic Resistance in Hepatocellular Carcinoma
ACS Nano ( IF 16 )
Pub Date : 2026-01-06
DOI: 10.1021/acsnano.5c11352
Yen-Nhi Ngoc Ta,Van-Anh Thi Nguyen,Thu-Thuy Can,Meng-Cheng Hsieh,Bang Giang Thi Cao,Dehui Wan,Chian-Hui Lai,Chun-Chieh Wu,Fu-Fei Hsu,Yu-Ting Yen,Shen-Nien Wang,Yunching Chen
 |
 |
 |
 |
| 二维材料Frontier | 生物纳米材料前沿 | MXenes Frontier | 纳米医学Frontier |
|
版权所有 © 2019 北京北科新材科技有限公司
All rights reserved. 京ICP备16054715号-2 |
扫一扫