Theranostics | Э̫ͬ����ƽ̨���ھ�����ѧ
QQѧ������Ⱥ��1092348845
��ϸ����
THz ���������������ʣ���ǵ�����䡢��ˮ�������Ժ�ָ��ʶ��Ԥ�ƽ�Ϊ������ѧ����ͻ�ơ�Ȼ����������ȱ�㣺�����dz��������Ѻ������ԣ����ٴ�Ӧ�ü�Ϊ���ޡ������������˽��ڿ�ѧ�ƽ�չ���� THz ��������Ͽ�ѧ�����������˹����ܣ�AI�������㽨ģ������༭�����ؼ������ϣ������ܹ�֧�ִ���������������־������Ƽ�⼰ҩ�����������ȫ����ѧ�������������Ϻ�����ϵͳ�����磬�� THz �볬���ϻ����ṹ��ϣ������������������־�����������;�˹������㷨�ܹ����١�ȷ�ؽ��������������ʵ���Զ������;�����غͻ��� CRISPR ϵͳ���ںϴ����˳�����Һ����ƽ̨����Щ�ۺϷ���������������м����ϰ�����Ϊʵ�־���ʵ���ٴ���ֵ�Ķ������ϵͳ�����˵�·��ͨ���ٽ���ѧ�ƺ�����THz �������Խ�һ���Ż���ʵ�ָ�ȷ����Ч���Ի��İ�֢����������DZ���ӻ����о�ת��Ϊ��ʵ������ٴ�Ӱ�졣

���о�����Ϊ��Synergistic terahertz platforms for precision oncology.��������Theranostics�ϡ�
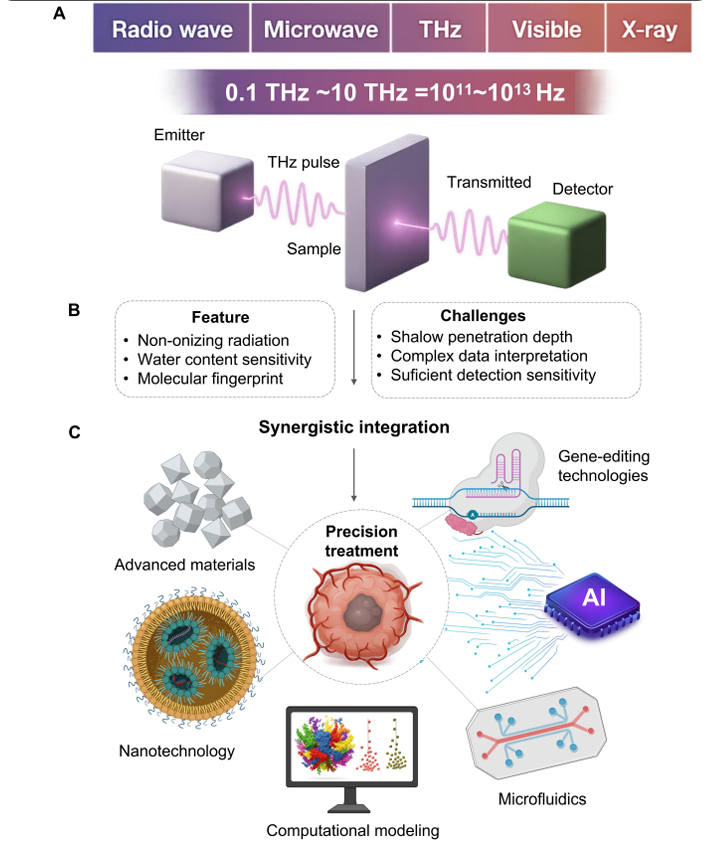
THz�ھ�����ѧ�еķ�չ������ָ���������Ĺؼ��㡢��������ޣ����ṩ�˻�������������Э���Կ˷���Щ��ս�Ĺ滮���ԡ�A. THz����λ����������֮���0.1��10 THz�ĵ����Χ�ڡ����͵�ʱ��ϵͳ����������������ķ���������Ʒ�Ҽ����������źŵ�̽������B. �ü���������ѧӦ���о��������������ܶȡ�ˮ���м�����ָ�����ԣ���Ȼ�����ٴ�Ӧ����������ս����֯�����ޡ����������������⡢���������־�����������Խϲ��C. ��THz�����������˹����ܡ����غͻ���༭���߽�ϣ��ɴ�������ƽ̨�����������������ȡ�����������Ϣ��ʵ�ַ����Զ������ṩ�������ƣ��ƶ�THz��DZ���ٴ�Ӧ�÷�չ��
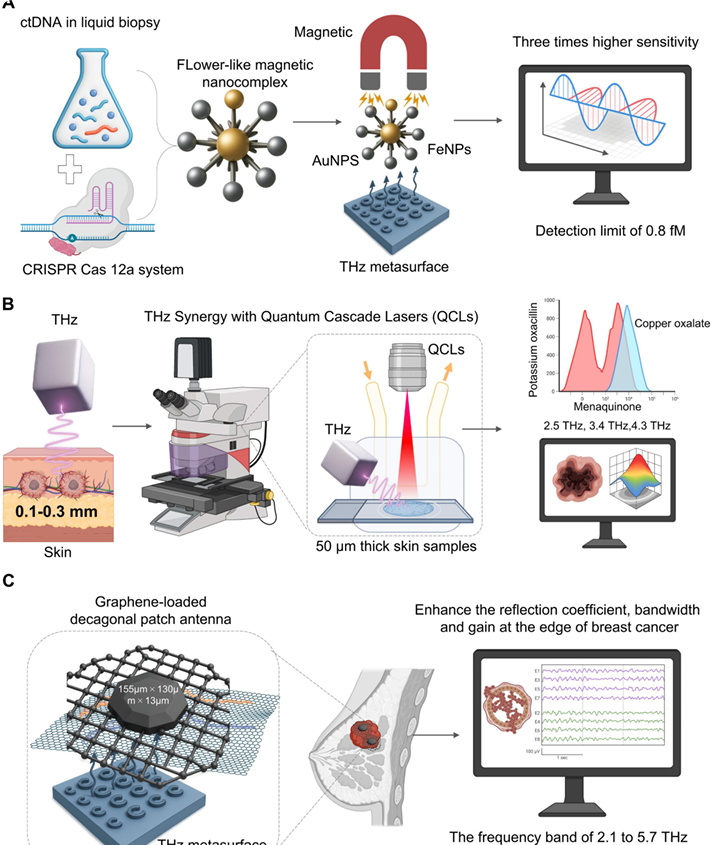
Эͬ��THzƽָ̨����֢��ϡ�һ�������CRISPR/Cas12a��ѭ��������ctDNA���������ϵͳ���ɻ�״�����������auP-FeNPs������THz���������Թ�����ص�����й�أ��ø�������յ�ǿ���λ�ƣ�����������ctDNA��0.8 fM��Ҫ���ߵ�THz�ź������ȡ�B.����THzdz��Ƥ������~0.1-0.3���ף�������ʹ��խ��QCLԴ���и߷ֱ��ʻ�ѧ����ϵͳɨ�象��֯��Ƭ��50�ף�����ɨ�貿�ַ��ӣ���ׅ�ͪ��2.5 THz����ͭ�����Σ�3.4 THz������ʾ�ޱ����֯����ѧ�о��������Ե����շ塣C.��ϻ���ʯīϩ��ʮ���ΰ߿����ߣ���ϵͳ��ǿ�˾ֲ���ų�������ʵ��2.1-5.7 THz�����ܡ����ṩ�˸��õķ���ϵ�������������棬�Ӷ�ʵ�ָ�������ϸ�ֵ����ٰ���⡣
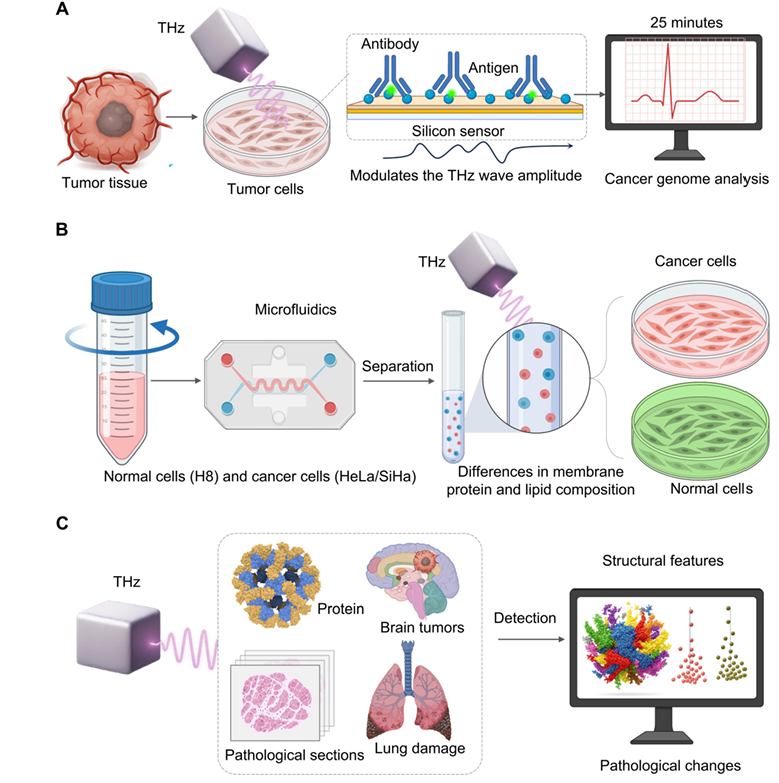
��̫���ȼ�����߾��Ⱥͼ���֧�ֽ�ϡ�A. ���ڿ�ԭ-�����ڹ贫�����ϵĽ��ģ�Ⱙ֢�������������ı�ֲ�����ܶȲ�����̫���Ȳ����ȡ������ʹ�ø߶ȴ�����������25�����ڼ��㰩ϸ����������ʵ�ֿ��ٻ�������ϡ�B. ʹ������оƬ������ͨ��̫���ȹ�������ϸ����H8���Ӱ�ϸ����HeLa/SiHa���з��롣̫���ȿ��Ը���Ĥ�ɷֻ�õ��ض����������������ǣ��Ӷ�ʵ���ޱ�Ǹ�ͨ��ϸ��������C. �����ʡ����������ͷ���֯�ĸ��Ӹ�ά�������˹������Զ��������˹������㷨�������۷������Է��ֵ��쳣ģʽ�Ͳ�����������Щͼ��ԭʼ̫��������ת��Ϊ��ȷ����Ϻ����Ʒ�����
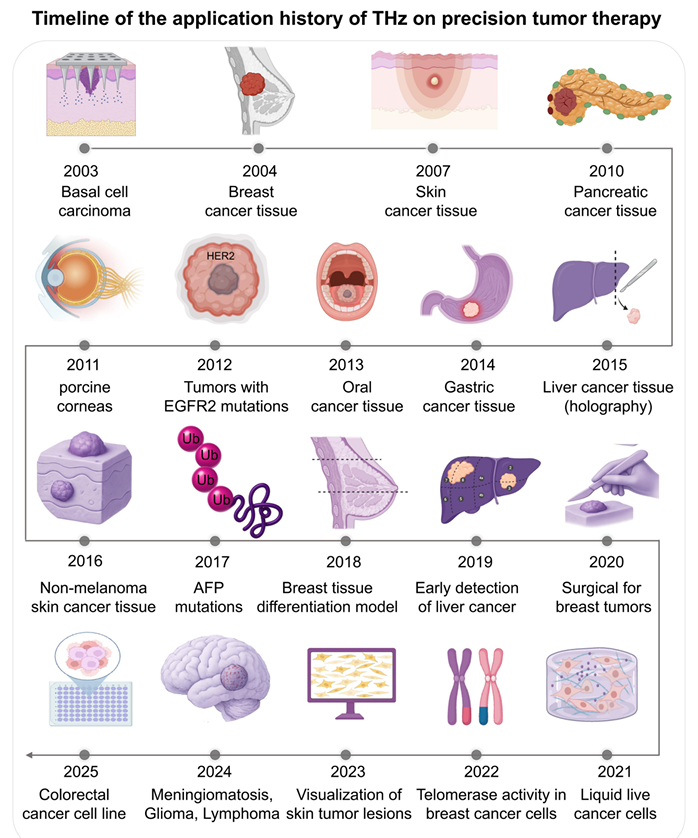
��THz�������ھ���֢��ϵ�Ӧ���У���һЩ�ؼ�����ʷ��̱���������о��Ƕ��г���֯���г�����ϸ���� 2003���������� 2004�������ʮ����о���չ��������֢�����ٰ�����ǻ����θ�����������־�HER2��2012���Լ�������������ȫϢ���� 2015�������������ٴ�Ӧ����������Ե��⣨2020����Һ���������2021������Ӳ��棨�����ø���Ե��أ��ѳ�Ϊǰ�ء��������ķ�չ����������Ƥ��������ӻ���THz������ת������2023������ʾ�˸��������ϵ����ơ��ɴ˱�����THz�����Ѵ�ʵ���ҵĺ������ݱ�Ϊ��ҽѧ�����DZ���ļ�����
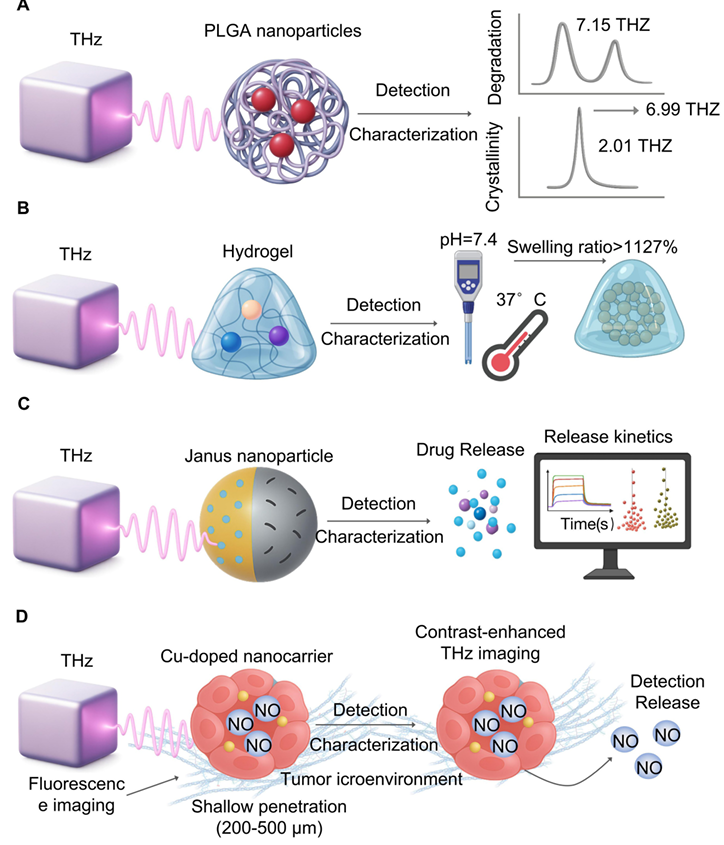
�������ҩ���ҩ����͡�A. ̫���ȹ����ܹ�ʵʱ����PLGA�����ľۺ�������壨7.15��6.99 THz���Ļ��Ա仯��Ӧˮ�⣬����ǿ�ȣ�2.01 THz����ӳ�ᾧ�ȱ仯����Բ������ܷdz���Ҫ��B. ̫���Ȳ������������£�pH 7.4, 37��C���������Ե��о�ˮ��״̬���Ӷ����Բ������ͱȵ����ʣ����ͱȿɳ���1127%������ҩ���ͷš�C. �����壨��˫��ӦJanus�����������ͷŶ���ѧ��ͨ��̫���ȱ�������������ʵ�ĸ����ͷţ����ṩ��ҩ������ϵͳ���õ���Ϣ��D. ̫���ȳ����ӫ�������������ǣ��������������е�ҩ��ֲ������������Է�ӫ�⣬���Ը��ã����ܸ������ؿ��ӻ������������Ϊ��
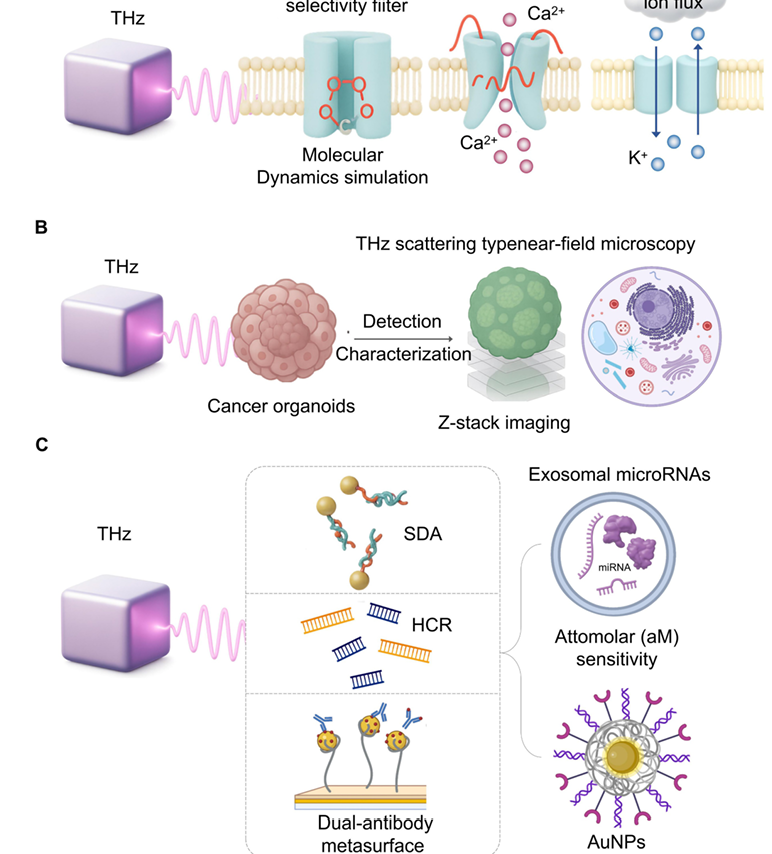
����̫����ʵ��ϸ�����ƺͳ��������ȼ�⡣A. ���Ӷ���ѧģ�������̫���Ȳ�����ֱ��������ͨ��ѡ������������ã��ı��乹����������ÿ�����ǿ��ͨ���������ͨ��ʧ�⣬Ϊ��ؼ��������һ����ӱ�ķ����������Ʋ��ԡ�B. ��̫����ɢ���ͽ���������Z��ѵ��������ϣ�����ʵ���ޱ�ǡ���ϸ���ֱ��ʵİ�֢�����ٷ��������ַ�������ӫ���Ǽ���Ϊ��ͨ���ٴ�ǰҩ��ɸѡ�ṩ��ϸ�Ľṹ��Ϣ��C. �ﵽҺ��������İ�Ħ���������ȣ���Ҫ��̫�������ﴫ�������źŷŴ�������ϡ��������û�������SDA���������������AuNPs����ϵ��ӽ�����Ӧ��HCR���Լ�˫���峬���漼���ȷ�����ʹ�ض�RNA�ij�����������Ϊ���ܡ�
�ܽ�
̫���ȼ�������ǵ��롢��ˮ���кͷ���ָ��ʶ������ԣ�����������������չ�ֳ�����DZ���������ٴ�ת�����������ڴ����dz�����ݽ������ӵȼ���ƿ�������ڷ����ڡ�Theranostics����һƪ����ϵͳ�����˶�ѧ�ƽ����ں�����ƶ�̫����ƽ̨ʵ��ͻ�ơ��о�ָ����ͨ����̫���������ײ��ϡ��˹����ܡ�����༭�����صȼ������ϣ��ɹ�������һ����������ϵͳ�����磬���ṹ��ǿ�ʹ���������������������־���������ȣ�CRISPR-Cas12aϵͳʹ��ѭ������DNA�ij�������Ϊ���ܣ�AI�㷨ʵ���˸��ӹ��Ŀ��ٽ������Զ���ϣ�������оƬ��֧�ֻ�ϸ�����ޱ�ǡ���ͨ����������ЩЭͬ���Բ��������̫�����������ȡ������������Ч�ʷ���Ĺ��о��ޣ�ҲΪ�������б߽�ȷ����������������ҩ���ͷż����������ͨ�����صȻ��ڿ�������·����
����̫���ȼ�������ʵ�����о���ȡ��ϵ�н�չ�����������ٴ�����������ЧӦ���Ʋ���ȷ�����ڰ�ȫ���д���֤���豸���ɶ����������Բ���ȶ�����ս��δ������ͨ����ѧ�ƺ��������������ﰲȫ������ϵ���̫������������ϵ����û��Ƶ��о������ƶ���Яʽ��һ�廯�ٴ��豸�Ŀ��������ż������ϳ������ģ̬ƽ̨�����ϣ�̫����������ʵ�ִӻ����о����ٴ�Ӧ�õĿ�Խ��Ϊ������������ϡ�����������Ч����ṩ����Ч����ȫ�Ĺ��ߣ������ƶ�������������Ի�����̬���ķ���չ��
�ο����ף�
DOI: 10.7150/thno.128658

 ѧ��ǰ��
ѧ��ǰ��