IF 16!使用铜递送 Co-N-C 单原子纳米酶通过代谢重编程增强铜质沉积
QQ学术交流群:1092348845
详细介绍
本文精选
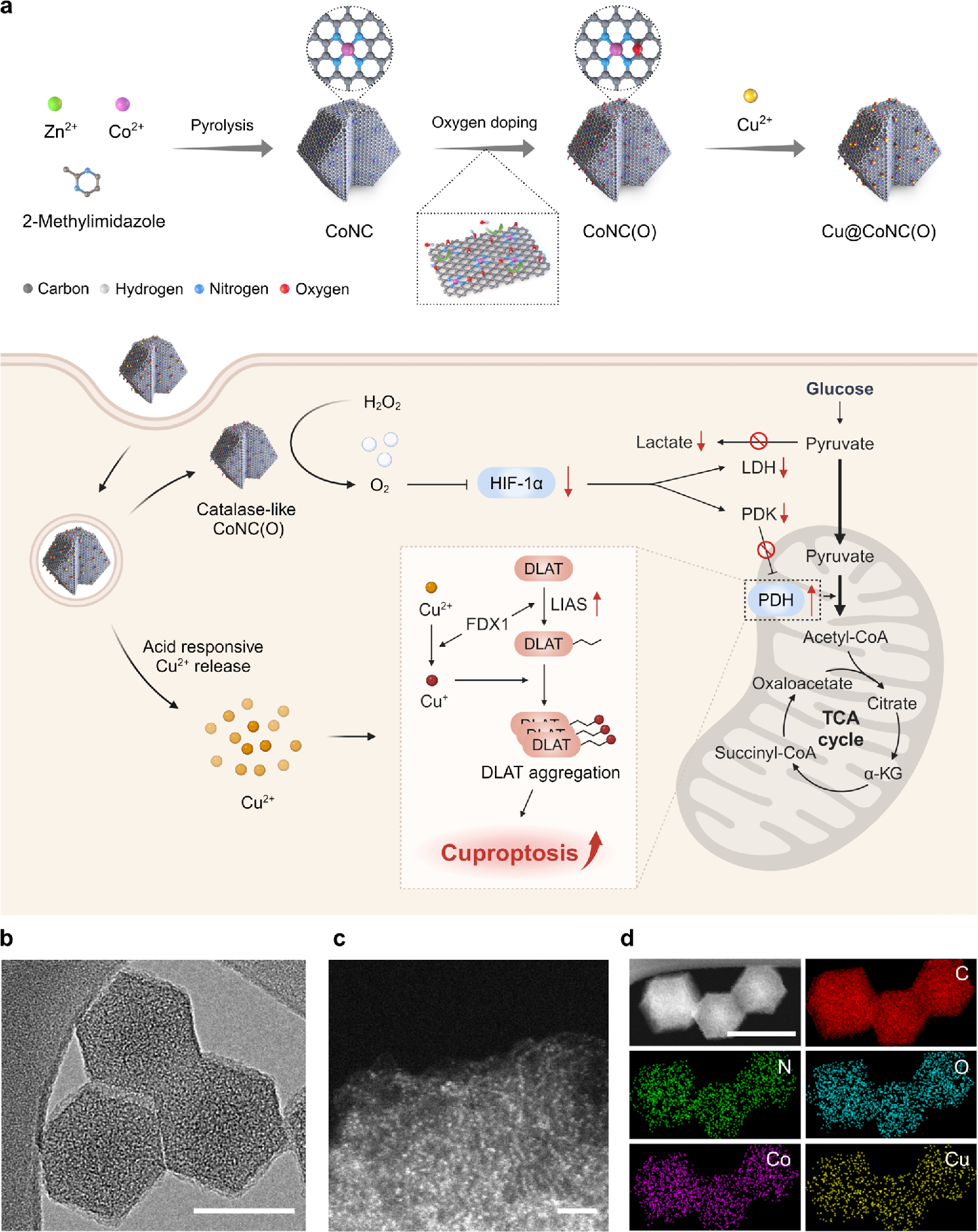
铜依赖性细胞死亡是一种铜依赖性细胞死亡,已显示出作为一种以线粒体蛋白聚集为特征的癌症疗法的前景。然而,这一独特的特征使其疗效高度依赖于癌细胞的代谢状态,在线粒体活性降低的缺氧肿瘤中产生不良预后。在此,我们使用富氧钴单原子纳米酶 (Cu@CoNC(O)) 构建了一种具有过氧化氢酶样活性的 Cu 递送载体,以在递送铜的同时重编程代谢。通过将含氧官能团引入碳载体上,Cu@CoNC(O) 与缺氧对应物相比,Cu 离子的负载效率显著提高。同时,Cu@CoNC(O) 出色的过氧化氢酶样活性可缓解缺氧,通过抑制乳酸代谢和激活丙酮酸脱氢酶复合物,将代谢从糖酵解转变为线粒体呼吸。即使在缺氧条件下,代谢转移和有效 Cu 递送的协同作用也能促进 Cuproposis,从而增强治疗效果。本研究证明了单原子纳米酶作为催化离子递送载体的潜力,能够同时执行催化功能和递送金属离子,提出了一种通过代谢调节增强 cupropsosis 的有效策略。
生物医学应用
该纳米酶平台通过代谢重编程策略,优先靶向线粒体异常/糖酵解依赖型肿瘤(如胰腺癌、肝癌、乳腺癌),联合放化疗/光热治疗增强疗效;兼具诊疗一体化功能(如铜基单原子纳米酶的PET成像),可实时监测载体分布与代谢变化,实现精准干预;拓展应用于神经退行性疾病(调节能量代谢/金属稳态)、缺血再灌注损伤(改善缺氧/代谢紊乱)、纤维化/感染性疾病(调控代谢重编程)等代谢相关疾病治疗。
原文链接
Enhanced Cuproptosis via Metabolic Reprogramming Using Copper-Delivering Co–N–C Single-Atom Nanozyme
ACS Nano ( IF 16 )
Pub Date : 2025-06-11
DOI: 10.1021/acsnano.5c00012
Kang Kim, Jaewoo Lee, Ok Kyu Park, Hyochul Lee, Taekyu Jang, Jungho Kim, Bowon Lee, Jeong Hyun Kim, Jaeho Moon, Seoin Back, Nohyun Lee, Seung Hong Choi, Taeghwan Hyeo
- 上一款: IF 10.9!集成 DNA 逻辑门控细胞膜
- 下一款: Advanced Functional Ma

 mxene 学术专题
mxene 学术专题